Наследники по кривой: биороботов научили размножаться
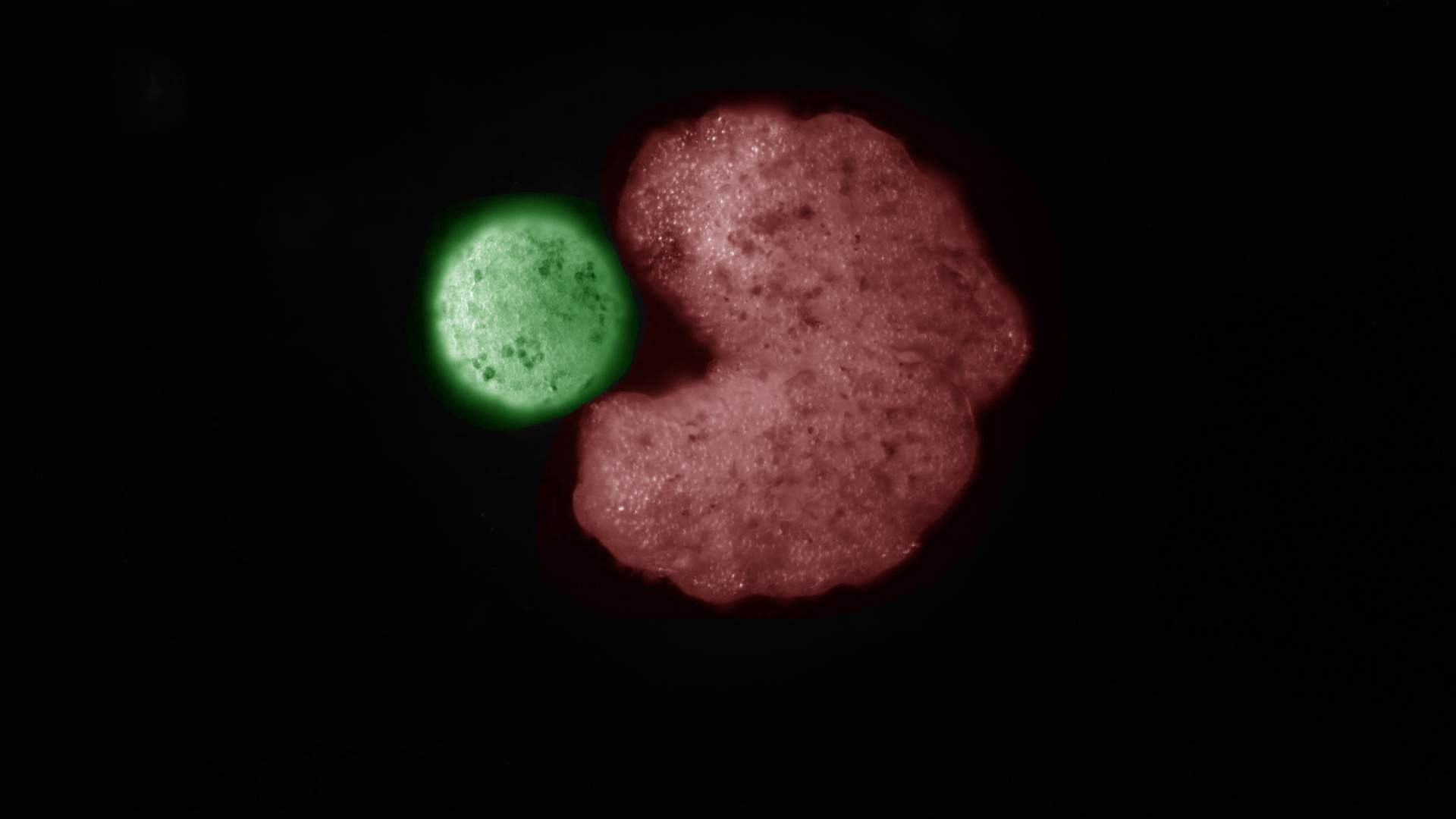
Биороботы из живых лягушачьих клеток могут размножаться неведомым миру животных и растений способом, заявили американские ученые. Ксеноботы, которым придали форму Пакмана из старинной компьютерной игры, и вовсе преодолели порог в одно поколение потомства. Стоит ли бояться самовоспроизводящихся микророботов, чем они в перспективе могут помочь людям и такое уж ли это уникальное явление, читайте в материале «Известий».
Плодовитый Пакман
Робота большинство людей представляет машиной из металла, которая, что важнее, выполняет определенные действия по воле человека, говорит профессор робототехники из Университета Вермонта и один из авторов исследования о ксеноботах Джош Бонгард. Ксенобот — тоже робот, хоть и созданный из эмбрионов лягушки.
Группа американских ученых обнародовала метод создания биороботов из живых клеток в январе прошлого года. «Организмы» размером примерно в миллиметр создали из клеток шпорцевой лягушки (Xenopus, отсюда и название). Каждому из них придавали форму вручную. В апреле этого года стало известно, что ксеноботы научились передвигаться по площадке, расчищают ее от мусора и даже восстанавливаются от травм.

В своей новой статье ученые сообщили, что биороботы продемонстрировали способность к самовоспроизведению, причем размножаются они способом, который не свойственен растениям и животным.
Наибольшую способность к созданию потомства в соответствии с расчетами ИИ показали 80-восьмидесятых Pac-Man. В отличие от «собратьев» иной формы они смогли воспроизвести до четырех поколений.
По словам авторов исследования, технология находится на ранней стадии развития. Однако уже сейчас они предполагают, что она может найти применение, в частности, в медицине и сфере защиты окружающей среды. «Известия» попросили российских ученых рассказать, можно ли считать результаты их американских коллег прорывом, где могут пригодиться ксеноботы и стоит ли бояться восстания роботов с приставкой «био».
Не такие уж удивительные
Анна Кудрявцева, кандидат биологических наук, замдиректора по научной работе Института молекулярной биологии им. В.А. Энгельгардта (ИМБ) РАН, заведующая лабораторией постгеномных исследований:
В нынешнем виде практическое использование этой разработки маловероятно. Но если изменить процедуру получения биоботов, оставив саму идею конструирования псевдоорганизмов, состоящих из разных типов клеток и нацеленных на выполнение определенных функций, я могу предположить три потенциальные области применения: это регенеративная медицина, адресная доставка веществ или клеток, а также лечение некоторых воспалительных процессов, ассоциированных с антибиотико-резистентными бактериями.
Первый вариант выглядит наиболее правдоподобным, в то время как остальные два имеют существенные ограничения, связанные с размерами таких биоботов, а следовательно, их способностью проникать сквозь ткани. Через кровоток их запускать едва ли возможно, так как это может вызвать закупорку сосудов.
Сейчас для получения биоботов используются клетки, которые должны стать во взрослом организме клетками кожи и сердечной мышцы, то есть определенным образом детерминированные, но вследствие раннего изъятия из эмбриона они еще сохраняют способность к многократному делению. Для применения в биомедицине необходимо будет отказаться от использования эмбрионов и перейти к перепрограммированию, процессу, при котором под влиянием активации нескольких генов (факторов Яманаки) соматические клетки переходят в состояние стволовых.
Этот способ не является новым для науки и давно используется для биомедицинских целей. Однако нельзя забывать, что подобные манипуляции могут таить в себе опасность онкологических заболеваний, потому как стволовые клетки, находящиеся не в «правильном» месте и в непривычном окружении, могут легко ошибиться и пойти в сторону усиленного размножения, а не дифференцировки.

Способность поглощать другие живые объекты, например, простейших или бактерии, также не является уникальной особенностью ксеноботов. В нашем организме некоторые клетки используют фагоцитоз (процесс клеточного пищеварения). Во взрослом состоянии этим занимаются, например, макрофаги, чтобы уничтожить потенциально опасные источники инфекции. А в младенческом возрасте именно внутриклеточное пищеварение помогает нам усваивать материнское молоко.
Более того, ксеноботы не являются формой жизни, которую совсем уж невозможно встретить в живой природе. Существуют похожие организмы, например, трихоплаксы, а также личинки кишечнополостных и губок. А если вспомнить биогенетический закон Геккеля–Мюллера о том, что онтогенез повторяет филогенез, а также то, что некоторые организмы смогли приобрести способность к размножению на личиночной стадии и стать отдельной систематической группой, то ксеноботы и вовсе перестают быть такими уж удивительными. Они напоминают фагоцителлу, которая, по теории Мечникова, являлась предком всех многоклеточных организмов.
Это следствие грамотно подобранных экспериментатором условий, а не уникальное биологическое явление. Я бы рассматривала исследование скорее в качестве демонстрации возможностей вычислительной биологии с применением эволюционных алгоритмов, нежели беспрецедентное научное открытие.
Пока что с уверенностью можно сказать только две вещи: до реального использования, даже если оно возможно, еще долго, и надо быть крайне осторожным, когда выпускаешь в естественную среду что-то искусственно созданное или нетипичное для данного конкретного места. Достаточно вспомнить борщевик в Московской области или камчатского краба в Баренцевом море в районе Мурманска.
Предложения использовать ксеноботов для сбора микропластика представляются мне необоснованными. Ведь даже если микропластик будет поглощаться ими путем фагоцитоза, то есть наподобие пищи, он же всё равно не сможет внутри полноценно перерабатываться, а значит, после нескольких этапов деления клеток ксенобот погибнет, микропластик вернется на свое место, а водоем получит дополнительную порцию органики, которая также не очень полезна для стабильности экосистемы.
Наследство лягушки
Александр Афонин, доцент, кандидат технических наук, декан факультета робототехники университета «Синергия»:
На сегодняшний день ксеноботы — это серьезное научное достижение американских ученых, демонстрирующее большие потенциальные возможности в направлении создания биологических роботов и искусственных организмов. Но одновременно это лишь первый успешный шаг на этом тернистом пути, подтверждающий, что природа задолго до появления человечества естественным путем сумела создать несоизмеримо более сложные биологические организмы, с потаенными комплексными механизмами работы которых мы зачастую еще только начинаем знакомиться.
По сути, американские ученые на базе стволовых клеток лягушки сумели сконструировать и изготовить биологическое устройство, или «организм», способный поддерживать собственную форму и какое-то время жить за счет биологической энергии, заранее накопленной в клетках. Естественная способность клеток слипаться между собой интерпретируется как возможность «залечивания ран». Поскольку помимо стволовых клеток эпителия (кожи) лягушки используется часть стволовых клеток ее сердечных мышц, «организм» приобретает возможность хаотичного движения в жидкой среде из-за их сокращений. Микрохирургическими методами придавая «организму» определенную форму, создатели улучшают его способность к движению, подталкиванию и даже сбору встречающегося на пути взвешенного в жидкости материала.

Если проводить аналогию с техническими устройствами, то мы имеем корпус с ковшом спереди, запас топлива и постоянно работающий грубо центрированный двигатель.
И вот такой микробульдозер описывает спиралеобразные траектории в тонком слое жидкости чашки Петри, раздвигая или собирая перед собой мусор или биоматериалы, иногда закручивая их в клубки... Когда кончается топливо, «организм» умирает и разлагается. Движения пока бессмысленны, скорее всего, вязкая жидкость демпфирует хаотичные метания, отфильтровывая среднее направление движения, поэтому складывается впечатление «осмысленности» круговых траекторий.
Систем связи, ориентации, навигации, управления нет, поскольку очевидно, что у «организма» отсутствуют органы чувств и центральная нервная система. Однако элементы вегетативной нервной системы, возможно, есть. И это не заслуга разработчиков устройства, а наследство от лягушки.
Речь, видимо, идет о чувствительных элементах эпителия, реагирующих на воздействие окружающей среды, активных клетках сердечной мышцы, управляющих ее сокращением, и других сложных механизмах, скрытых в исходном живом биологическом материале, включая, возможно, отмеченную учеными способность «организмов» к пока не самой удачной саморепликации — упрощенному самовоспроизведению на базе имеющегося вокруг, собираемого ими аналогичного биоматериала, а также к некоторому взаимодействию или скорее коммуникации (взаимным реакциям) с себе подобными «организмами» и другими объектами.
Выдвинутые рядом авторов предположения о том, что в будущем ксеноботы или их «потомки» найдут широкое применение в области регенеративной медицины или очистки природы от многочисленных и разнообразных загрязнений, пока преждевременны, хотя и не безосновательны. Конечно, после глубокой доработки эта микробиомашина в будущем может найти самое разнообразное применение. В том числе в разрешении фундаментальных проблем медицины и экологии, да и ряда других областей — сельского хозяйства и промышленности, строительства и транспорта, и еще много-много чего.

Она же может стать грозным оружием и средством безопасности, а когда-нибудь даже, может быть, последней надеждой человечества и даже жизни на Земле. Но мы этого еще не знаем. Не знаем мы, и какие подводные камни и даже опасности таит в себе это направление исследований и разработок, к чему может привести массовое появление, использование, распространение и развитие подобных организмов. Ответ на эти вопросы может дать лишь наука и практика.
Без шансов на восстание
Тимур Чернов, научный сотрудник лаборатории молекулярно-биологических и нейробиологических проблем и биоскрининга МФТИ, старший преподаватель департамента молекулярно-биологической физики МФТИ:
Говоря о возможном медицинском применении зарождающейся технологии, можно выделить несколько направлений, в рамках которых планируется вести разработки: что-то где-то удалить, что-то где-то нарастить, что-то куда-то отнести и что-то где-то синтезировать (непосредственно внутри организма). Стоит оговориться, что подобные частицы необходимо создавать на основе клеток самого пациента: так мы предотвратим проблему отторжения, а внесение генетических изменений позволит придать им необходимые терапевтические свойства.
Различные нарушения обмена могут приводить к локальному накоплению тех или иных веществ. Создав живые частицы, способные к переработке этих веществ, и снабдив их способностью к правильному таксису (направленное движение в ответ на раздражитель), мы сможем удалять тромбы или холестериновые бляшки в сосудах. Высокодоходный рынок косметологии будет заинтересован возможностью создания самореплицирующихся частиц, способных удалять подкожные жировые отложения — без операций, упражнений и прочих трудностей.

С помощью подобной технологи также можно помогать при ожогах, переломах позвоночника и ряде других травм.
Еще одна потенциальная сфера применения — адресная доставка лекарственных препаратов. Зачастую мишенью препарата, который распространяется через кровоток, является конкретное место или ткань, а его присутствие во всем организме при этом нежелательно. Это приводит к широкому спектру побочных эффектов, а также повышению общей нагрузки на организм, связанной с необходимостью утилизации и выведения лекарственных препаратов. Частицы, запрограммированные двигаться к какому-то заданному месту (очагу воспаления, раковой опухоли и т. д.), помогут применять препарат более локально, а это позволит существенно снизить дозировку и снизить побочные эффекты.
Кроме того, ничто не мешает внедрить в подобные частицы гены, отвечающие за синтез необходимых организму веществ. Системы обратной связи позволят синтезировать строго необходимое количество в конкретный момент времени. Это может послужить хорошим решением для патологий, требующих так называемой заместительной терапии. К примеру — диабет первого типа. Запрограммированные частицы могли бы поддерживать необходимые концентрации инсулина в организме.
Говоря о других сферах применения, стоит отметить, что самореплицирующиеся организмы могли бы собирать микропластик, формируя его в крупные конгломераты, которые уже могли бы отбирать различные приборы. Но нам известно большое количество ферментов, способных расщеплять микропластик до молекул, которые, в свою очередь, могут выступать в роли питательных веществ. Так, данная технология имеет потенциал к созданию репликантов, способных к биодеградации созданных человеком полимеров.
В ближайшем будущем широко будет обсуждаться вопрос: а не выйдет ли эта технология из-под контроля? Так происходит каждый раз с появлением новой технологии. Кроме того, массовая культура давно рисует нам образы взбесившихся репликантов, которые уничтожают всё на своем пути, преследуя лишь одну цель — создать как можно больше собственных копий. Если вернуться к реальности, можно узнать, что ученые давно уже отработали методы решения этой проблемы.
Можно выделить два основных подхода: «несамостоятельность» организмов и запрограммированное самоуничтожение. В первом случае в создаваемый организм вносится запланированный недостаток, чаще всего заключающийся в невозможности самостоятельно синтезировать какое-то вещество, необходимое для роста и функционирования. Есть второй вариант: на стадии проектирования в геном добавляются гены, воспроизведение которых приведет к самоуничтожению организма. Так что подобные опасения напрасны.
Перемотка эволюции
Павел Кривозубов, руководитель направления «Робототехника и искусственный интеллект» Кластера информационных технологий Фонда «Сколково»:
В первую очередь процесс, подобный саморепликации, наводит на прямую аналогию с ядерной реакцией. Вполне возможно, с помощью таких механизмов и самореплицирующихся роботов можно будет вырабатывать энергию, пусть и не в таких масштабах, как ядерный реактор. Такой сценарий применения технологии может быть возможным при решении ряда проблем, связанных с циклами «размножения» подобных роботов.
Второй вариант — очищение и восстановление продуктивности полигонов бытовых отходов. Если сейчас возможно запустить процесс замещения одних клеток на другие, то такого рода саморепликационная модель может применяться для переработки больших объемов биомусора или даже пластика. В процессе такой переработки одни клетки замещаются другими.
Также ксеноботов можно будет применять в исследовательских целях, например, для исследования эволюционных процессов. Теоретически мы сможем многократно ускорять процессы, которые в нормальном их течении занимают миллионы лет, и проследить какие-либо эволюционные изменения.
На данный момент подобные технологии еще не достигли такого этапа развития, но в будущем это не исключено.
Один из возможных вариантов применения технологии в исследованиях и на практике — использование механизмов саморепликации для регенерации тканей человека. Это станет доступным, если мы научимся управлять процессом и получать необходимый результат, и это не будет вызывать отторжения организма при трансплантации.
С точки зрения экологии, это действительно будет полезно, например, для очистки Мирового океана. Как мы знаем, есть определенный ряд проблем, связанных с экологическим состоянием: на ряде участков Атлантического и Тихого океанов наблюдаются огромные «острова» из пластика, которые, к сожалению, остаются после человеческой деятельности и попадают в Мировой океан. Эти технологии могут в будущем помочь избавиться от таких проблем.











