С помощью зонда: нанокапилляры помогут создать лекарства будущего

Российские ученые создали уникальную методику исследования строения и свойств живых клеток. Они предложили новые инструменты, подходящие одновременно для многих типов молекулярных исследований, — модифицированные серебряными частицами нанокапилляры. Их использование в доклинических исследованиях улучшит точность оценки силы воздействия на ткани как вредных факторов, так и новых методов лечения, уверены специалисты.
Наносеребряные пули
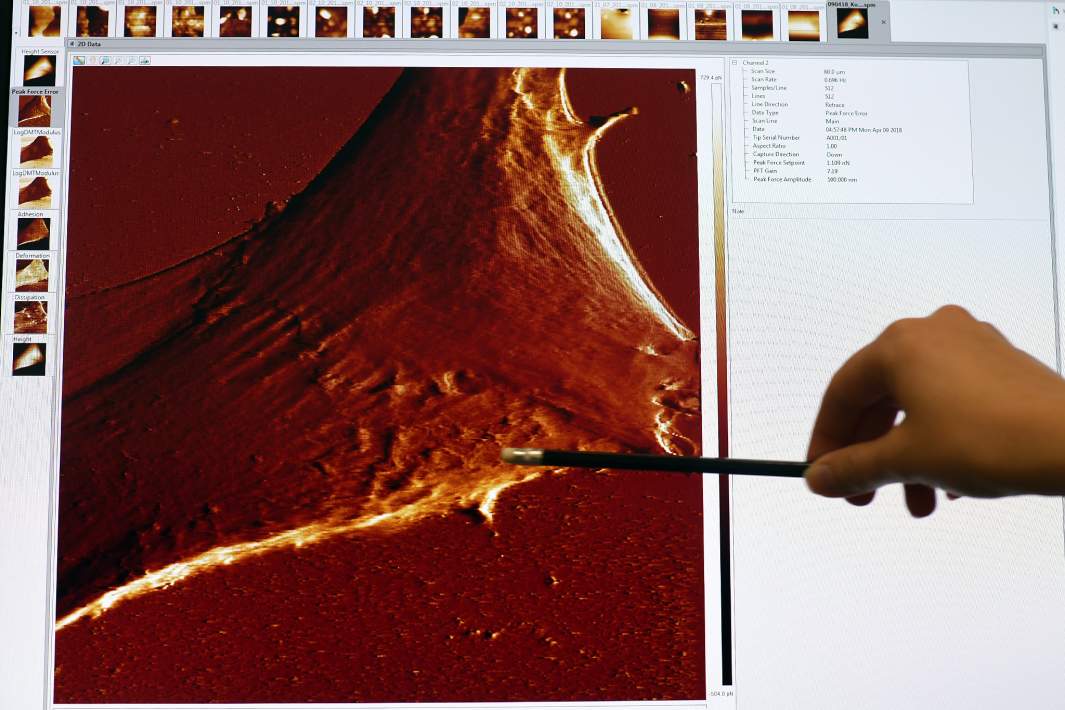
Коллектив ученых Института перспективных материалов и технологий (ПМТ) МИЭТ совместно с коллегами из научно-исследовательской лаборатории биофизики МИСИС разработал модифицированные серебряными наночастицами нанокапилляры. Об этом «Известиям» сообщили в пресс-службе Минобрнауки. Это миниатюрные зонды, которые могут сканировать и визуализировать поверхность живых клеток, и одновременно с этим наноразмерные «шприцы», позволяющие вводить в эти клетки лекарство, не повреждая их.
Метод будут использовать для доклинических исследований новых лекарственных препаратов. Нанокапилляры позволят повысить точность сканирования топографии (пространственного расположения) живых клеток и измерения их механических свойств, а значит и улучшить оценку силы воздействия на них как вредных факторов, так и новых методов лечения различных болезней. Возможность изучения многих параметров с одновременным получением механических характеристик и визуализации живых клеток позволит существенно расширить инструментарий ученых, рассказал «Известиям» доцент Института ПМТ МИЭТ Сергей Дубков.
— Такой модифицированный нанокапилляр можно использовать для регулирования доставки молекул или ионов и для изучения in vivo (в живых тканях) их воздействия на живую клетку, — сказал эксперт.
Наночастицы позволят повысить точность сканирующей ионно-проводящей микроскопии (СИПМ), которая визуализирует отдельные молекулы с нанометровым разрешением. К настоящему времени СИПМ зарекомендовала себя как отличный инструмент для сканирования живых опухолевых клеток, нейронов и белков с указанным разрешением. Также их можно использовать для анализа молекулярного состава цитоплазмы и ядра живых клеток. Речь о методе спектроскопии гигантского комбинационного рассеяния (ГКР) света, которая обладает уникальной чувствительностью и обеспечивает обнаружение и идентификацию одиночных молекул.
— Модификация поверхности нанокапилляра серебряными наночастицами усовершенствует этот инструмент и помимо визуализации живых клеток и анализа их механических свойств позволит с его помощью анализировать также биологические процессы, протекающие в клетках, — то есть проводить более глубокую комплексную диагностику клеток и существенно сократить время доклинических исследований новых лекарственных препаратов, — пояснил Сергей Дубков.
Новый инструмент позволит проводить исследования со сверхчувствительным обнаружением аномалий в живых клетках, изучать молекулярный состав мембраны, цитоплазмы и ядра в зависимости от клеточной линии-мишени или внешних эффектов, таких как взаимодействие с лекарствами, изменение температуры и так далее.
Практическое использование
Ожидается, что новая методика может войти в практику исследований в течение пяти – семи лет. С помощью нее можно будет создавать противоопухолевые лекарственные средства и другие препараты.
— Совместно с научным коллективом МИЭТ мы разработали метод совмещенного ГКР-анализа живых клеток с применением уникальной научной установки — сканирующего ион-проводящего микроскопа, который есть только в НИТУ МИСИС, — отметил инженер научного проекта лаборатории биофизики НИТУ МИСИС Василий Колмогоров.
По его словам, метод уникален тем, что одновременно можно изучать морфологию и локальные механические свойства, а также ГКР-спектры отдельных внутриклеточных функционально различных областей. Разработанная методика в перспективе будет применяться для скрининга эффективности новейших терапевтических препаратов.
Использование разработанной методики перспективно, полагает главный научный сотрудник Института физики твердого тела им. Ю.А. Осипьяна РАН Владимир Кукушкин. По его словам, несмотря на значительные успехи развития современной медицины, исследования механизмов влияния лекарственных препаратов на отдельные клетки, а также изучение биологических процессов и метаболизма здоровых и злокачественных клеток требуют дополнительного использования новых подходов.
— Применение модифицированного нанокапилляра позволит обеспечить возможность безвредного получения в реальном времени информации как о механических характеристиках, так и о протекании внутренних химических процессов и составе живой клетки. Кроме того, благодаря нанометровым размерам острия капилляра его введение и извлечение не будет нести вреда для клетки, обеспечивая возможность введения лекарственных препаратов в заданных концентрациях или взятия пробы для последующего анализа, — сказал эксперт «Известиям».
Эти возможности позволят с высокой точностью анализировать воздействие лекарственных препаратов, а также заранее обнаруживать возникновение накопительных эффектов, потенциально способных привести к возникновению патологий и раковых опухолей, резюмировал Владимир Кукушкин.
Однако, по мнению ряда экспертов, методика новая и еще должна зарекомендовать себя в дальнейших исследованиях.
Работы проводятся в рамках программы развития университета «Приоритет 2030». Исследование выполнено при поддержке Российского научного фонда, посвященного разработке многофункциональной платформы для фенотипирования раковых клеток. Результаты научной работы опубликованы в спецвыпуске «Достижения сканирующей зондовой микроскопии в клеточной биологии» международного научного журнала Cells.